Lungemboli (LE) är ett underdiagnostiserat tillstånd. 50% av alla patienter med proximal DVT har samtidig LE och 70% av alla patienter med LE kan man påvisa samtidig DVT på (1). Man uppskattar att 90% av alla lungembolier härstammar från DVT (1).
Sannolikheten för LE ökar vid förekomst av riskfaktorer för venös tromboembolism. Endast 20% av patienterna saknar predisponerande faktor (idiopatisk LE) (1).
| Predisponerande faktorer för venös tromboembolism (VTE) (1) |
| Starka predisponerande faktorer OR > 10 |
Moderata predisponerande faktorer OR 2-9 |
Svaga predisponerande faktorer OR < 2 |
| Höft- eller benfrakturHöft- eller knäprotes.Stor kirurgi.
Stort trauma.
Ryggmärgsskada. |
Tidigare VTE.Trombofili.Paralytisk stroke.
Kronisk hjärt- eller lungsjukdom.
Malignitet.
Kemoterapi.
Central venkateter.
Artroskopisk knäkirurgi.
Hormonersättning. P-piller.
Graviditet / post partum. |
Sängliggande > 3 dagar.Lång resa (flyg eller bil).Hög ålder.
Lapraskopisk kirurgi.
Övervikt.
Graviditet / antepartum.
Åderbråck. |
Symptom
I 95 % av fallen kan den kliniska bilden vid lungemboli hänföras till något av följande tre symptombilder:
- Akut dyspné inkl ångest.
- Pleuritsmärta eller hemoptys.
- Högerkammarsvikt med eller utan chockbild eller synkope.
Övriga symptom som bör föranleda misstanke om lungemboli
- Oklar försämring vid annan sjukdom trots behandling (t ex hjärtsvikt, KOL)
- Oklar subfebrilitet
- Oklar arytmi, t ex nydebuterat förmaksflimmer
- Oklar syncope
- Recidiverande ”pleuropneumoni”
- Oklara bröst/buksmärtor
Diffdiagnoser
| Akut dyspné |
Pleuritsmärta |
Högersvikt |
Chock |
Hemoptys (ovanligt vid LE, endast 10%) |
| AstmaHjärtsviktPneumothorax
Pneumoni
Bronkit |
PleuritPerimyokarditPneumothorax
Pneumoni
Tumör
Subfrenisk abscess |
InfarktTamponadMyokardit
Pneumoni vid KOL |
InfarktBlödningTamponad
Sepsis
Aortadissektion
Ventilpneumothorax |
TumörPneumoniMitralisstenos
Bronkit
Tbc |
Utredning
Utredningen av misstänkt lungemboli är behäftad med diverse svårigheter. Samtidigt som tillståndet är underdiagnostiserat och potentiellt letalt kan man inte utreda alla. Värdera symptom och riskfaktorer. Ta hjälp av nedanstånde diagnosticum. Om annan trolig förklaring till insjuknande saknas stärks behovet av utredning men om mer trolig genes till symptomen finns kan oftast denna behandlas och vid förbättring stärker detta den initiala diagnosen. Vid utebliven förbättring bör lungemboliutredning övervägas.
Klinisk bedömning
Den kliniska sannolikhetsbedömningen är central i utredningen av misstänkt LE. Enl socialstyrelsen skall Wells score användas. Revised Geneva score finns också att tillgå. I de båda scoringsystemen är risken för LE 10% vid låg, 30% vid intermediär och 65% vid hög klinisk misstanke (1).
| Wells score (1) |
Revised Geneva score (1) |
| Tidigare VTE |
1,5 |
Ålder > 65 år |
1 |
| Nylig kirurgi eller immobilisering |
1,5 |
Tidigare VTE |
3 |
| Malignitet |
1 |
Kirurgi eller frakut inom 1 mån |
2 |
| Hemoptys |
1 |
Aktiv malignitet |
2 |
| HF > 100 slag/min |
1,5 |
Unilateral bensmärta |
3 |
| Klinisk misstanke om DVT |
3 |
Hemoptys |
2 |
| Alternativ diagnos mindre trolig |
3 |
HF 75-95 slag/min |
3 |
|
HF ≥ 95 slag/min |
5 |
| Ömhet över djupa vener eller unilateralt ödem |
4 |
Sannolikhet (3 nivåer)
- Låg (0-1 p)
- Intermediär (2-6 p)
- Hög (≥ 7 p)
|
Sannolikhet (3 nivåer)
- Låg (0-3 p)
- Intermediär (4-10 p)
- Hög (≥ 11 p)
|
| Sannolikhet (2 nivåer)
|
Vid låg klinisk sannolikhet kan PERC-score användas (2). Vid negativ PERC-score är sannolikheten för LE så låg så att riskerna med att kontrollera D-dimer är högre än eventuella vinster. Regeln kan användas om sannolikheten för LE bedöms < 15 % och Wells score < 2 p. Om samtliga kriterier är uppfylld (< 1,8% risk för LE) finns det mer att förlora än att vinna på att ta en D-dimer (kontrast, strålning, bifynd, blödningsrisk etc). Regeln kan inte användas i Europa (?) eftersom vår pretest-sannolikhet är för hög här (20-30%???).
PERC Score
- Ålder < 50 år
- HR < 100/min (patienter med betablockerare var exkluderade i orginalstudien).
- Saturation > 94% på rumsluft
- Ingen tidigare VTE
- Inget trauma / kirurgi senaste 4 veckorna
- Inte hemoptys
- Inte östrogen / P-piller
- Ingen ensidig bensvullnad
Kemlab
- Blodgas. Det klassiska utseendet är sänkt pO2 (hypoxi) och sänkt pCO2 (hyperventilation). Blodgasen kan dessvärre se ut hur som helst. Glöm inte att 20% av patienterna med LE har normalt pO2 (1).
- D-dimer. Redan innan man ordinerar D-dimer bör man tänka efter vad man tänker göra med svaret. Ett negativt D-dimer talar starkt emot LE (hög sensitivitet med högt negativt prediktivt värde) medan ett positivt D-dimer kan bero på många olika sjukdomar (låg specificitet med lågt positivt prediktivt värde). ELISA-analyserad D-dimer har en sensitivitet på > 95% och en specificitet på 40% (< 10% vid ålder > 80 år) (1).
- Om symptomen började > 1 v sedan kan D-dimeren vara falskt negativ.
Fyslab
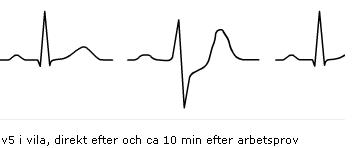
EKG. Tecken till högerkammarpåverkan kan ses såsom T-vågsinversion V1-V4, QR i V1, klassikern S1Q3T3 eller inkomplett eller komplett högersidigt skänkelblock (1).
UKG. Avsaknad av fynd av högerkammarpåverkan vid ultraljudsundersökning hos en patient i chock utesluter lungemboli som orsak (3).
Radiologi
Lungröntgen kan visa fynd i form av atelektas eller pleuravätska. Röntens viktigaste funktion är att utesluta andra orsaker till dyspné såsom hjärtsvikt eller pneumoni.
Definitiv diagnos
- Ultraljud ben. Sensitivitet på 90% och specificitet på 95% avseende proximal DVT (1). Hos patienter med LE påvisas DVT med ultraljud i 20-50% av fallen (1). Används framför allt när scint inte kan göras pga lungsjukdom och DT angio är olämpligt pga njursvikt.
- Lungscint eller perfusion- ventilationsscintigram. Sannolikheten för förekomst av LE klassificeras som 1) Normal, 2) Låg-, 3) Intermediär- och 4) Hög risk. Normalt fynd har högt negativt prediktivt värde. Används vid ålder < 45 för att undvika joniserad strålning (och kontrast) men har i princip inga andra fördelar.
- DT-angio. Spiral-DT har en sensitivitet på 83% och specificitet på 96% (1). Vid låg eller intermediär klinisk risk enl Wells har negativ DT-angio högt negativt prediktivt värde. Om negativ DT-angio kan utesluta LE vid hög klinisk misstanke och om isolerade subsegmentella embolier vid låg klinisk misstanke skall behandlas debatteras altjämnt. Används vid ålder > 45 år samt när snar scint inte finns tillgänglig (helgtid).
Handläggning
Patientens tillstånd får avgöra handläggningens hastighet, logistik och paralell behandling. Behandlingen bör inte styras av hur utbredd emboliseringen är på pulmonalisangion eller scinten utan snarare patientens kliniska status (1). En ung patient med starkt hjärta klarar en större embolisering utan att krokna än en äldre patient.
Beställ diagnostik. Om hög sannolikhet och/eller lång väntan tills röntgen ges LMWH innan undersökningen (halv eller hel dygnsdos beroende på sannolikhet och väntetid). En variant kan vara att ge halv fulldos innan. Vid cirkulatorisk påverkan eller hög blödningsrisk ges hellre Heparin (om trombolys kan bli aktuellt) dosen är 5000 E iv (7500 E om vikt > 90 kg). Obs kort halveringstid (1-2 tim).
När diagnosen är klar sätts Waran eller NOAK in. Fragmin ges i minst 5 dagar om Waran väljs. Patienten bör vara kvar på sjukhus tills saturationen förbättrats och patienten klarar av att komma hem, rimligen 3-5 dagar efter diagnos. Vid HK-påverkan bör pat ligga i telemetri för att fånga ev arrytmier. En helt stabil patient kan polikliniseras vid låg PESI-score (klass I PESI < 65, klass II PESI < 85). Då bör också TNT vara negativt.
| Riskstratifiera patienterna efter 30-dagarsmortalitetsrisk (1). |
| Riskkategori |
30 dagarsmortalitet |
Klinisk bild |
| Högrisk |
15% |
Hemodynamisk svikt |
| Intermediärrisk |
3-15% |
Högerkammarpåverkan (UKG) ellerHjärtmuskelskada (TNT) |
| Lågrisk |
< 1% |
Klinisk stabilitetAvsaknad av HK-påverkanInga tecken till hjärtmuskelskada |
Stabil hemodynamik
BT >100 mmHG, puls <100
Ge patienten Fragmin i behandlingsdos och skicka remiss för definitiv diagnos enligt ovan. Denna kan vänta till morgonen efter om patienten kommer kvällstid.
Mindre embolier
Ej central embolus eller <40 % perfusionsdefekt
- Sedvanlig behandling med LMWH + Waran eller NOAK.
Massiv lungemboli
Central embolus eller >40 % perfusionsdefekt
- Dessa patienter har ofta en nedsatt högerkammarfunktion vilket kan bekräftas med ekokardiografi. De har oftare EKG-förändringar och ev också TNT-förhöjning.
- Om nedsatt högerkammarfunktion övervägs trombolys (eftersom proppen är mer lucker än trombosen vid ST-höjningsinfarkt kommer effekten betydligt snabbare men blödningsrisken är klart högre pga konsumtion av koagulationsfaktorer).
- Om trombolys väljs förordar somliga heparindropp medan andra föredrar LMWH i 2-dos. Rationalen är att kunna sätta ut/pausa blodförtunningen om blödning uppkommer.
- Om trombolys avstås rekommenderas LMWH i 2-dos (Innohep 100 E/kg k v x 2).
Instabil hemodynamik
BT <100 mmHG, puls >100, allmänpåverkan
Överväg akut trombolys på vitalindikation där differentialdiagnos kan uteslutas. Om man kan avvakta säker diagnos görs denna först, lämpligen pulmonalisangio eller UKG. Ge LMWH eller bolusdos Heparin iv (se ovan) + starta ev heparininfusion i väntan på beslut.
Trombolys
Inj Alteplas (Actilyse®) 10 mg i.v. bolus + 90 mg iv under 2 tim. Vid vikt < 65 kg ges en sammanlagd dos om 1,5 mg/kg (3). Vid hjärtstopp orsakat av lungemboli kan alteplas 50 mg ges som bolus (3) och HLR bör fortgå en tid efter för att ge läkemedlet en chans att verka. Ges på HIA i Jönköping (4).
Om beslut om trombolys inte kan tas genast ges behandling med heparininfusion (5000 E om vikt < 90 kg alt 7500 E om vikt > 90 kg alt 80 E/kg iv som bolus + inf 500 E/Kg/dygn dvs 18E/kg/tim) i avvaktan på beslut.
Gör uppehåll med heparininfusion under trombolys, och börja igen 60 min efter avslutad Actilyse-infusion utan heparinbolusdos. Alternativt ges Innohep i 2-dosförfarande under 2 dygn med start 2 tim efter avslutad trombolys (om minst 12 tim om fulldos gavs innan trombolys) (4).
Övrig behandling
Understödjande
- Syrgas
- Vätsketillförsel
- Ev inotropt stöd.
Mobilisering och symptomlindring
- Sängläge endast vid uttalade symptom eller hemodynamiskt påverkad patient. I övrigt fri mobilisering.
- Paracetamol vid måttlig smärta. Vid uttalad pleuritretning kan tillägg av kortverkande NSAID eller Cox 2-hämmare vara av värde under några dygn.
Sekundärprofylax
| Trombofilidefekt ej påvisad |
Behandlingstidens längd |
| Lungemboli, första |
6 mån |
| Kvarstående besvär efter 6 mån – förläng till |
12 mån |
| Recidiverande idiopatisk lungemboli |
12 mån–tills vidare |
I vanlig ordning vägs recidivrisk mot blödningsrisk. Se Tillstånd som predisponerar för VTE för detaljer.
Uppföljning
Patienter som vid sexmånaderskontrollen inte har full funktionskapacitet, d v s blir mer andfådda vid ansträngning än före lungemboliinsjuknandet skall utredas vidare med lungröntgen, ev perfusionsscint och UCG med tanke på pulmonell hypertension.
AVK –behandlingen förlängs i dessa fall 6-12 månader i avvaktan på utredning och nytt ställningstagande.
Komplikationer
Den akuta mortaliteten vid LE är så hög som 7-11% (1).
0,5-5% av patienter med behandlad LE får pulmonell arteriell hypertension (PAH) (1).
Recidivrisken vid idiopatisk lungemboli är minst 25 % under 5 år.
Sannolikheten för att nästa VTE-episod är en ny LE är 60%.
Referenser
- Torbicki A: Guidelines on the diagnosis and management of acute pulmonary embolism. European Heart Journal 2008;2276–2315
- Kline JA, Mitchell AM, Kabrhel C, et al. Clinical criteria to prevent unnecessary diagnostic testing in emergency department patients with suspected pulmonary embolism. J Thromb Haemost. 2004;2:1247-1255.
- Mokhtari – ABC om chock på akuten – 2015.
- Tufvesson I: Lungeomboli. Föreläsning medicinkliniken 2020.